作者:李佳
审校:张洁 孙超
单位:天津医科大学总医院消化内科
编者按
肝脏是人体重要的代谢器官,负责解毒、产生胆汁、储存营养物质并调节多种代谢过程。维持正常的肝细胞功能需要精细的线粒体质量控制(MQC),包括线粒体分裂、融合、生成及自噬等多个环节。研究表明,线粒体功能障碍与多种急慢性肝病的发生发展密切相关,如酒精相关性肝病(ALD)和代谢相关脂肪性肝病等。然而,线粒体功能障碍如何影响肝病中的炎症通路和细胞死亡的具体机制仍不明确。近日,天津医科大学总医院孙超教授团队在International Journal of Biological Sciences杂志(IF:8.09)发表了一篇文章,针对MQC在肝脏疾病中的作用进行了综述。本刊特邀请进行撰文,为我们详细介绍MQC,分析不同有害因素引发线粒体功能障碍的机制,并进一步阐明了MQC失衡如何促进肝病的发生发展,最终提出以线粒体为中心的治疗策略。

文章发表
(doi:10.7150/ijbs.107777)
线粒体及其功能
线粒体是由双层膜构成的细胞器,负责多种重要的细胞功能,如葡萄糖和脂质代谢、细胞增殖与死亡、能量供应和先天免疫反应。通过氧化磷酸化(OXPHOS),线粒体产生ATP,供应约90%的细胞能量。能量底物进入线粒体基质,通过三羧酸循环生成电子载体(如NADH和FADH2),这些电子载体通过电子传递链(ETC)传递电子,推动质子泵将质子从基质转移到膜间隙,建立电化学梯度。ATP合酶利用质子梯度将ADP磷酸化为ATP。此外,线粒体还参与铁代谢、细胞增殖调节,并通过调控先天免疫反应在控制炎症及相关疾病进展中发挥重要作用。
MQC
MQC涉及多个过程的精细调控,包括线粒体动力学、生成和降解,这些过程对维持细胞稳态至关重要。
01
线粒体动力学(分裂与融合)
线粒体分裂主要由动力蛋白相关蛋白1(Drp1)介导,而线粒体融合则涉及线粒体融合蛋白1(MFN1)、线粒体融合蛋白2 (MFN2)和线粒体内膜融合蛋白1 (OPA1),它们分别介导线粒体外膜和线粒体内膜的融合。线粒体分裂促进后续的降解,而融合则保持线粒体DNA(mtDNA)的完整性。线粒体分裂与融合的动态平衡对维持线粒体功能至关重要。分裂过度会导致线粒体碎片化,影响能量生成和细胞功能;而融合过度则可能导致线粒体功能异常,影响细胞的适应性反应。在肝脏疾病中,线粒体动力学的失衡往往与炎症、纤维化和细胞凋亡密切相关。
02
线粒体生成
线粒体的生成受到核转录因子的调控,包括核因子相关因子1、核因子相关因子2和过氧化物酶体增殖物激活受体γ共激活因子1α(PGC-1α)。PGC-1α通过与核受体或激活转录因子相互作用,促进线粒体生物发生。线粒体生成失调与肝脏疾病尤其是非酒精性脂肪性肝病(NAFLD)的发生密切相关。在NAFLD小鼠和细胞模型中,沉默信息调节因子1(SIRT1)和PGC-1α的水平降低,导致细胞活力下降、凋亡增加、脂质积累和活性氧(ROS)生成增加。线粒体生成是维持细胞能量稳态的关键过程。当线粒体生成受到抑制时,细胞能量供应不足,导致细胞功能受损。在肝脏疾病中,线粒体生成的失调往往与脂质代谢异常、氧化应激增加和炎症反应加剧密切相关。
03
线粒体降解
线粒体降解的途径多种多样,包括泛素-蛋白酶体系统、线粒体自噬等。线粒体自噬通过自噬体介导的清除过程,选择性去除过剩或损伤的线粒体。研究表明,线粒体自噬与肝病的关系密切,包括NAFLD、ALD和病毒性肝炎。在NAFLD中,肝细胞的线粒体去极化现象表明功能早期失调,随之触发线粒体自噬,这一过程同样在细胞、小鼠和人类模型中得到证实。线粒体自噬是维持线粒体质量的重要机制。当线粒体受损时,自噬系统会选择性清除这些损伤的线粒体,防止其释放有害物质,如ROS和mtDNA,从而保护细胞免受进一步损伤。
这些协同作用形成了一个动态网络,通过MQC在能量匮乏或线粒体损伤时恢复稳态。图1展示了MQC的调节机制。
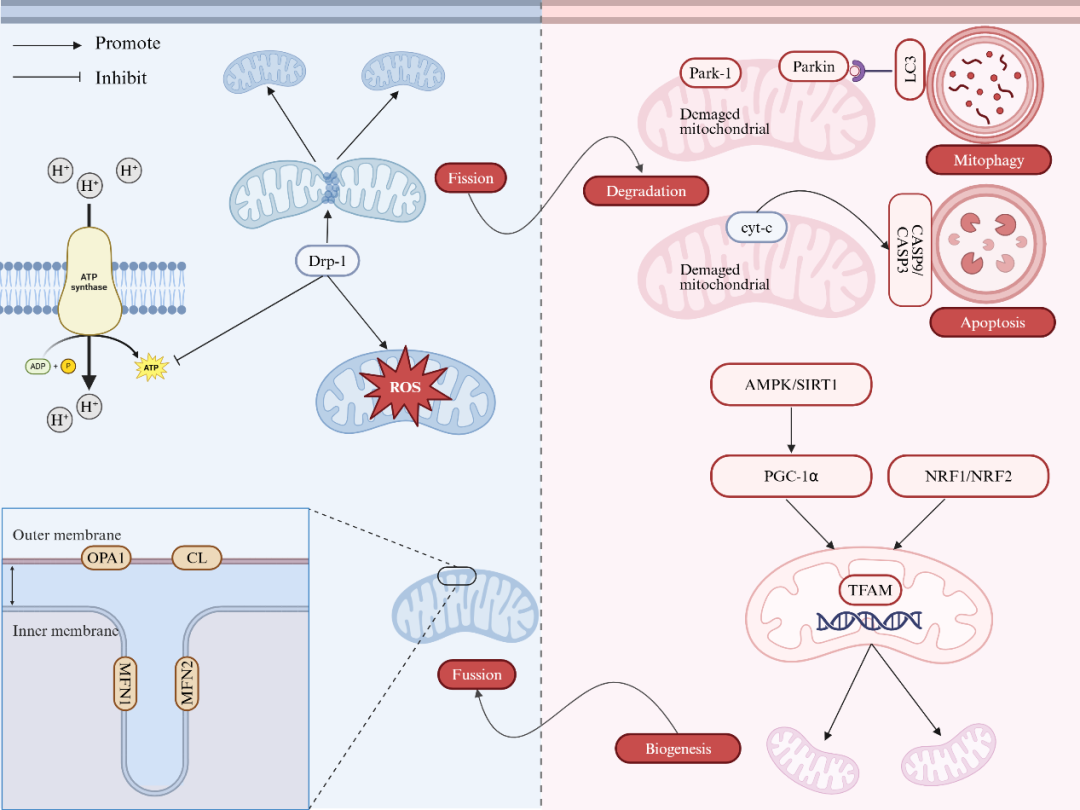
图1. 线粒体质量控制的调节机制
肝病常见病因与线粒体功能障碍的关系
01
病毒感染
乙型肝炎病毒(HBV)和丙型肝炎病毒(HCV)感染可导致线粒体形态和动力学的改变。HBV感染可导致细胞骨架破坏及线粒体形态异常,如嵴消失和线粒体肿胀。线粒体动力学的变化表现为Drp1表达上调,促进Parkin转位,增强线粒体分裂和自噬。线粒体分裂的增强降低了ATP生成,并干扰了钙离子流动,促进病毒的持续感染。此外,Drp1的过表达通过促进固醇调节元件结合蛋白1和PGC-1α的乙酰化,增强新生脂肪酸合成并抑制脂肪酸氧化(FAO),从而促进肝细胞癌细胞中的有害脂质积累。病毒感染对线粒体功能的影响不仅限于形态和动力学的改变,还涉及线粒体代谢的紊乱。HBV和HCV感染会导致线粒体OXPHOS功能受损,ATP生成减少,进而影响细胞的能量供应。此外,病毒感染还会引发线粒体ROS的过度生成,导致氧化应激增加,进一步加剧肝脏损伤。
02
饮酒
过量饮酒是ALD的主要诱因之一。乙醇通过影响线粒体的分裂与融合平衡,导致其结构改变,如大线粒体和线粒体碎片的形成。乙醇还通过刺激p53介导的Drp1表达,加剧线粒体分裂过程,导致线粒体功能障碍。长期饮酒通过提高NADH/NAD+比率,干扰线粒体生物合成,降低SIRT1活性,最终导致线粒体功能障碍。乙醇在肝脏中的代谢主要通过氧化途径和非氧化途径进行,其中乙醛是一种高度反应性的代谢产物,能够与蛋白质和DNA形成加合物,特别是在线粒体内,乙醛的大量积累会引发过度的氧化应激,造成肝脏损伤。乙醇对线粒体的影响不仅限于结构和功能的改变,还涉及线粒体代谢的紊乱。乙醇代谢过程中产生的乙醛和ROS会损害线粒体膜和mtDNA,导致线粒体功能进一步受损。此外,乙醇还会抑制线粒体脂肪酸氧化,导致脂质在肝细胞中的积累,进而引发脂肪变性和纤维化。
03
肥胖及肝脏代谢紊乱
肥胖与脂质稳态失调密切相关,导致脂质在肝细胞中的异位沉积。肝细胞中过量的脂质刺激线粒体的FAO,导致ROS的过度产生,形成恶性循环。过量的ROS损害线粒体功能,表现为线粒体嵴的丧失、基质的稀疏、OPA1和MFN1/2水平的降低,以及Drp1表达的增加,最终损害OXPHOS功能,并加剧ROS的生成。在NAFLD的体内外模型中,已经广泛观察到线粒体自噬功能缺陷,揭示了肝脏线粒体自噬缺失与NAFLD发生之间的密切关系。肥胖引起的线粒体功能障碍不仅限于脂质代谢的紊乱,还涉及炎症反应的加剧。过量的ROS会激活炎症小体,促进促炎细胞因子的释放,如IL-1β和TNF-α,进而加剧炎症损伤和纤维化。此外,肥胖还会导致线粒体自噬抑制,进一步加剧其损伤和肝脏疾病的进展(图2)。
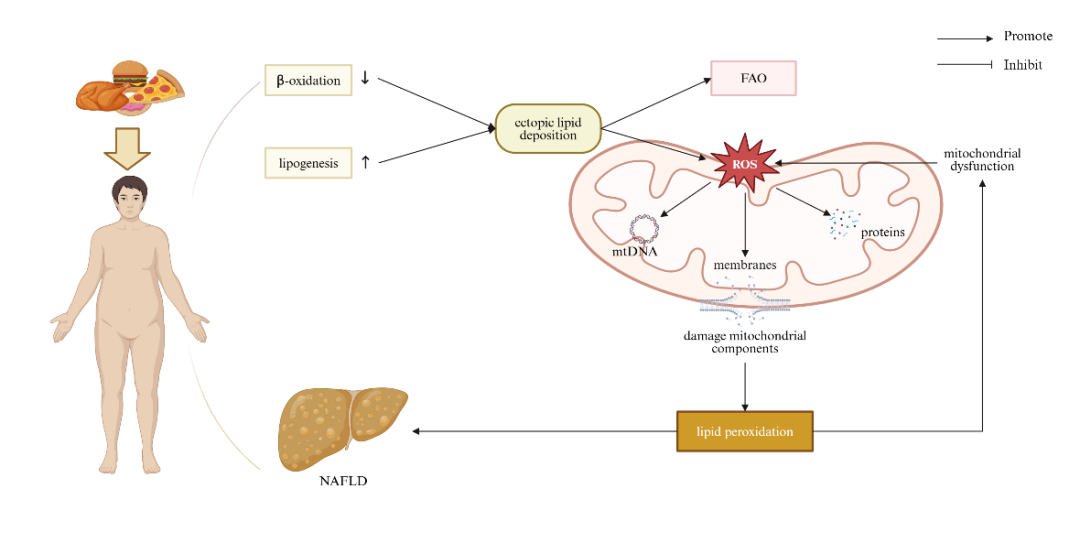
图2. 线粒体功能障碍与肥胖/NAFLD之间的关系
MQC受损的结果和肝病发生发展的关系
01
氧化应激和肝病
线粒体功能障碍导致过量的ROS生成,这也是导致各种肝脏损伤发病机制的主要因素之一。ROS的过度产生会触发NF-κB的激活,促进炎症和细胞存活基因的表达。过量的ROS积累可导致IL-1β和TNF-α等促凋亡细胞因子的上调。此外,ROS还可激活肿瘤抑制蛋白p53,继而刺激BCL-2相关X蛋白(Bax)的表达,Bax是线粒体孔形成的强效激活因子,进一步推动细胞的凋亡机制。氧化应激不仅影响线粒体膜和蛋白质,还会损害mtDNA,进一步导致缺陷线粒体蛋白的产生,破坏呼吸链的完整性,并加剧氧化应激。此外,ROS还会激活炎症小体,促进IL-1β和IL-18的释放,进一步加剧肝脏炎症和纤维化。
02
异常自噬和肝病
线粒体自噬通过多个信号通路调控,包括Pink1/Parkin通路、BNIP3L/Nix通路和FUNDC1通路。抑制线粒体自噬可促进巨噬细胞中mtDNA的释放,激活cGAS/STING/NLRP3信号通路,诱导促炎细胞因子的产生,加剧损伤。此外,mtDNA及ROS通过激活炎症小体,促进IL-1β和IL-18的分泌,进一步加剧炎症反应。线粒体自噬的失调不仅影响其清除,还会导致细胞内炎症反应的加剧。当自噬功能受损时,损伤的线粒体会积累并释放mtDNA和ROS,激活炎症小体和先天免疫反应,促进病损。
03
肝病中巨噬细胞异质性的时空维度
肝脏巨噬细胞在对不同刺激的反应中表现出显著的异质性,依据微环境和病理条件的不同,它们可以呈现促炎性的M1样或抗炎性的M2样表型。线粒体功能障碍是肝脏疾病发病机制,尤其巨噬细胞中的关键因素。受损的线粒体在巨噬细胞中释放mtDNA和ROS,激活炎症小体。在NAFLD和肝纤维化中,巨噬细胞中的线粒体功能障碍可能导致其极化向促炎性M1表型转变,加剧TNF-α和IL-1β等细胞因子的释放。巨噬细胞的极化亦受线粒体动力学的影响。在肝脏炎症的背景下,在巨噬细胞中受损的线粒体释放mtDNA和ROS,激活炎症小体。这一炎症级联反应不仅加剧了肝损伤,还加速了肝纤维化的进程。
药物靶向MQC治疗肝病
鉴于线粒体功能在多种肝脏疾病发病机制中的关键作用,旨在调节MQC的治疗策略具有极大的前景。本文讨论了靶向MQC治疗肝病的潜在策略(表1)。例如,Mdivi-1作为一种有效的线粒体分裂抑制剂,通过降低Drp1的磷酸化水平,抑制肝脏巨噬细胞的促炎反应;AICAR(AMPK通路的激动剂)则能够减轻肝纤维化的程度;槲皮素通过清除线粒体ROS并促进PGC-1α介导的线粒体稳态,进而保护肝细胞。尽管许多研究仍处于动物或细胞模型阶段,但药物靶向MQC在肝病治疗中展现了广阔的应用前景。
表1. 以线粒体质量控制为靶点的治疗策略

结论
MQC在维持肝脏健康和预防肝脏疾病的发生发展中至关重要。深入研究不同病理生理条件下与MQC相关的复杂机制,将为治疗干预开辟新方向。未来的研究聚焦于线粒体靶向治疗,可能为肝脏疾病的预防和管理提供创新策略,从而实现更好的临床治疗效果。
原文链接:Li J, Liu W, Zhang J, Sun C. The Role of Mitochondrial Quality Control in Liver Diseases: Dawn of a Therapeutic Era. Int J Biol Sci 2025; 21(4):1767-1783.
专家简介

孙超
天津医科大学总医院消化内科
副主任医师,本科毕业于北京大学医学部,天津医科大学医学/理学博士,日本兵库医科大学研究员。CNSLD第五届全国委员,中国人体健康科技促进会门脉高压专委会委员,中国营养学会高级会员,天津市互联网医学科普协会肝病学专委会副主任委员,天津市睡眠研究会青年委员会常委。
主持完成国家自然科学基金一项。执笔以及参与4部临床指南/专家共识的编写,担任SCI期刊JCTH编委,高起点新刊PH&C编委、高起点新刊eGastroenterology首届青年编委。在EASL年会、APASL年会、JSH总会、KASL年会做口头发言,在AASLD年会做壁板展示,指导学生在ACN(亚洲营养大会)做壁板展示。获得EASL的“Full Bursary”、APDW的“Travel Grant”、APASL的“Investigator Award”以及KASL的“Travel Award”奖励。以通讯作者在Clinical Nutrition, Briefings in Bioinformatics, Liver International, Cell Death & Disease等杂志发表SCI文章近80篇,他引1606次,h指数23,研究成果被ASGE(美国胃肠内镜学会)和EASL发布的临床实践指南引用、相关营养不良论著被New England Journal of Medicine(影响因子96.3)引用。
研究方向为细胞死亡/线粒体紊乱在肝损伤中的作用机制,体成分异常、营养不良、衰弱、睡眠障碍以及微量营养素对肝硬化/代谢相关脂肪性肝病的影响及干预措施。
第一作者

李佳
山西医科大学五年制临床医学专业,天津医科大学硕士研究生在读。以第一/共同第一作者身份发表SCI文章2篇,在APASL做口头发言、壁报展示,目前研究方向为代谢相关脂肪性肝病与膳食维生素摄入的关联、线粒体功能紊乱在肝脏疾病中的作用机制。

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
