当前位置:EASL-欧洲肝脏研究协会年会 » 正文
EASL热评 | 王炳元教授:借助全基因组分析,“解锁”酒精肝肝硬化预后
—— 作者: 时间:2021-03-25 01:44:46 阅读数:
24

韩白乙拉 内蒙古通辽市传染病医院
王炳元 中国医科大学附属第一医院
编者按:酒精性肝病(Alcoholic liver disease, ALD),又称为酒精相关性肝病(Alcohol-related liver diseases, ALD)在西方国家占慢性肝病的大多数,也是我国肝硬化的第二大常见病因。在EASL2020年会上,英国格拉斯哥健康与生命科学学院的学者通过全基因组分析(GWAS)分析了英国50万40-69岁人群的宿主基因分型和健康行为数据,发现6个基因与发生酒精相关性肝硬化的风险显著相关(大会摘要号:LBO05),结果引人关注。本刊特邀中国医科大学附属第一医院王炳元教授针对该项研究进行了精彩点评。

ALD是一种复杂的疾病, 酒精依赖和严重的酒精相关性肝损伤的易感性是由许多体质、环境和遗传因素决定的,尽管它们之间相互作用的性质和程度仍不清楚。大多数酗酒者会发展成脂肪变性,但只有少数人会发展为酒精性肝炎(10%~35%)和肝硬化(15%),一旦形成肝硬化,每年发生肝细胞癌的风险为1%~2%。尽管饮酒发生肝细胞癌的风险低于其他肝病的病因(如HBV),但它主要威胁青壮年。
环境因素如饮酒方式、并存肝病、肥胖、饮食结构和其他成瘾物质(包括烟草)等都可能改变ALD的自然病程。双胞胎研究揭示了遗传因素对ALD的进展起着重要作用,单卵双胞胎和双卵双胞胎的ALD的一致性高出非双胞胎的3倍。
随着基因分型技术的广泛应用,大量的基因病例对照研究评估了编码参与酒精代谢相关酶类的候选基因,如乙醇脱氢酶(ADH)、乙醛脱氢酶(ALDH)和细胞色素P450(CYPIIE1)等,介导宿主抗氧化防御,坏死性炎症和细胞外基质的形成和降解的进化和对抗。这些基因的多态性影响了宿主体内的酒精代谢,但主要是在东亚血统的个体中得到证实。
近年来进行的全基因组分析(Genome-Wide Association Study,GWAS),已经鉴定出三个强有力的候选基因PNPLA3、TM6SF2和MBOAT7的变异在ALD疾病谱中的作用。特别是PNPLA3(rs738409)的基因序列变异与肝甘油三酯积聚(脂肪变性)、炎症、纤维化、肝硬化,甚至肝细胞癌有关,目前被反复确认为ALD进展的第一个强有力的遗传危险因素(P=1.54×10-48);而MBOAT7(P=1.03×10-9)和TM6SF2(P=7.89×10-10)基因的变异是新的ALD危险位点。
酒精相关性肝癌中也存在特异性基因突变模式,包括CTNNB1、TERT、ARID1A和smarc2。此外,通过下一代测序在核苷酸水平上观察到的一个特定的突变过程揭示了酒精和烟草在肝癌发展中的协同作用。除此之外,还发现了与平均血小板体积(MPV)、平均红细胞体积(MCV)和血小板计数(PC)相关联的约500000个单核苷酸多态性(SNPs)基因型,其中5个主要基因组区的21个SNP与MCV、2个SNP与MCV和1个SNP与PC区有统计学意义(P<5x10-8)。
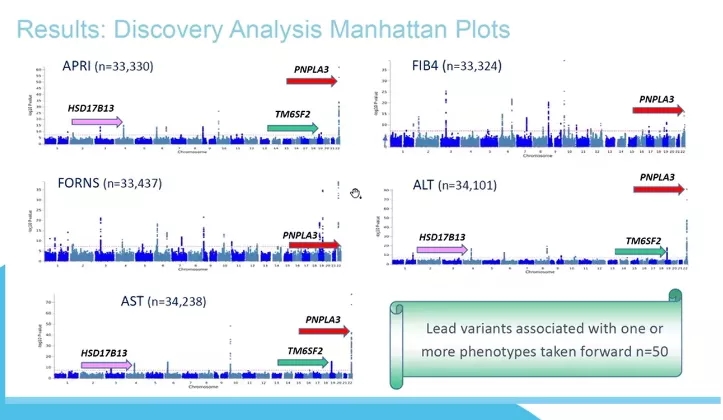
在本年度EASL会议上,英国格拉斯哥健康与生命科学学院的研究团队,整合了英国50万40-69岁人群的宿主基因分型和健康行为数据,以及生物化学变量的可用数据,受试者女性饮酒量>250 g/w,男性饮酒量>360 g/w,肝纤维化(APRI,FIB-4,Forn评分)和肝细胞损伤间接标志物(ALT、AST)的数据,调整年龄、性别、2型糖尿病和BMI后对这些受试者进行了GWAS分析。
研究者首先在3个独立的欧洲队列(第一阶段验证队列,n=2545)中,对发现分析中确定的基因与酒精相关性肝硬化的相关性进行了测试。在验证中,与酒精相关性肝硬化相关的变异体的错误发现率低于20%,然后在另外两个欧洲验证队列中直接进行基因分型(第2阶段验证,n=2068)。结果确定了50个具有全基因组显著性的独立危险位点(P值<5×10-8)。
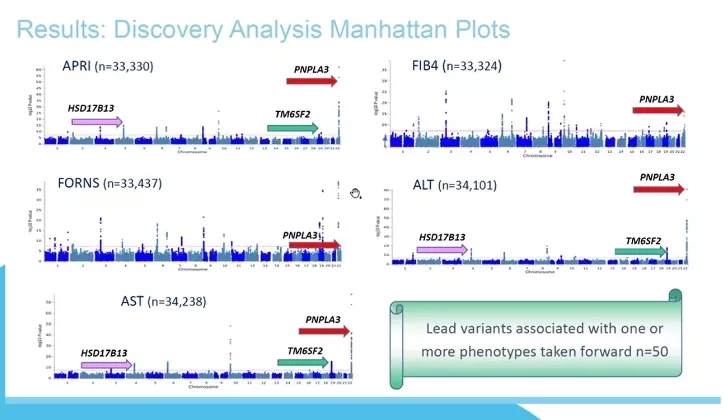
在第1阶段验证中,9个基因与发生酒精相关性肝硬化的风险显著相关;在第2阶段验证中,9个基因中的6个与发生酒精相关性肝硬化的风险显著相关。这6种基因包括PNPLA3、TM6SF2、HSD17B13和SERPINA1等4种已知风险变异体,新发现的2个风险变异体:线粒体胺肟基还原组分1(marc1)和不均一核核糖核蛋白U 样1(HRNPUL1)。
有趣的是,MARC1的次要a等位基因:rs2642438与酒精相关性肝硬化的风险降低相关(校正后的优势比为0.76;P=0.0027),HNRNPUL1:rs15052的次要c等位基因与酒精相关性肝硬化的风险增加相关(调整后的优势比为1.30;P=0.020)。
这些基因变异产生风险的机制以及它们之间功能相互作用的性质仍有待进一步确定,但一旦阐明,无疑将增加我们对ALD病理生理学的理解,而且对ALD危险因素的研究、ALD的临床结局的预测等均具有很好的参考作用。
专家简介

王炳元 教授
中国医科大学附属第一医院消化内科
中国医师协会脂肪肝专家委员会 副主任委员
中国医师协会肝病科普专家委员会 副主任委员
中国老年医学学会消化分会 常委
中国医药生物技术协会慢病管理分会 常委
中华消化学会老年协作组 副组长
中华消化学会肝胆学组 委员
中华肝病学会遗传代谢性肝病协作组 委员
辽宁省免疫学会老年免疫分会 主任委员
辽宁省基层卫生协会消化疾病防治专委会 主任委员
(来源:《国际肝病》编辑部)
标签:
新知
酒精性肝病
发表评论
全部评论